Prova de Concurso para Professor (Química) com Gabarito
Prova de Concurso para Professor (Química) com Gabarito
Concurso: SEED-PR - 2020 - Edital nº 47
Órgão/Instituição: Secretaria de Estado da Educação do Paraná
Banca/Organizadora: Centro Brasileiro de Pesquisa em Avaliação e Seleção e de Promoção de Eventos
Cargo: Professor - Química
Escolaridade: Nível Superior
QUESTÃO 01
CRESPE 2021: A água e o ácido sulfídrico são moléculas semelhantes, porque o oxigênio e o enxofre pertencem à mesma família da Tabela Periódica; ambas as moléculas apresentam duas ligações e geometria angular. Porém, as temperaturas de ebulição dessas duas substâncias são muito diferentes, conforme demonstrado a seguir.
TE (H2O) = +100 °C
TE (H2S) = −60 °C
Essas diferenças entre as temperaturas de ebulição das substâncias podem ser explicadas pela(o)
A) massa molecular das substâncias: a água tem massa molecular maior que a do ácido sulfídrico.
B) geometria das moléculas: como elas possuem diferentes arranjos espaciais, a molécula de água faz mais interações entre as moléculas, aumentando a temperatura de ebulição.
C) interação que ocorre entre as moléculas: na água são formadas ligações de hidrogênio, interações mais fortes que a interações dipolo-dipolo no ácido sulfídrico.
D) tamanho das moléculas: como o enxofre é maior que o oxigênio, isso faz que a molécula precise de mais energia para mudar de estado de agregação.
E) número atômico: como o oxigênio possui menos prótons no núcleo que o enxofre, ele então possui menos interações, por isso tem menor temperatura de ebulição.
QUESTÃO 02
CRESPE 2021: Variedades alotrópicas são as formas com que um elemento químico se apresenta na natureza como substância simples.
No caso do oxigênio, ele é encontrado na natureza de duas formas alotrópicas diferentes: O2 e O3. Nesse caso, a variação ocorre pela quantidade de átomos na molécula, mas existem variedades que se dão pela estrutura cristalina do composto.
Assinale a opção que apresenta duas variedades alotrópicas de estrutura cristalina.
A) S(rômbico) e S2
B) P (branco) e P (vermelho)
C) C (grafite) e C (diamante)
D) O2 e O3
E) S2 e S4
QUESTÃO 03
Internet: <www.infoescola.com>.
CRESPE 2021: A propanona, cuja fórmula estrutural é mostrada anteriormente, é um composto orgânico que pertence à função das cetonas. Esse solvente é comercializado como acetona, um removedor comum de esmaltes utilizado em salões de beleza. A respeito da propanona, é correto afirmar que o carbono da carbonila possui geometria
A) linear.
B) angular.
C) trigonal plana.
D) octaédrica.
E) tetraédrica.
QUESTÃO 04
CRESPE 2021: Os modelos atômicos tentam explicar como é a estrutura de um átomo, já que este é uma partícula muito pequena que não pode ser vista a olho nu. Até hoje, os cientistas não conseguiram ver um átomo isolado, muito menos a sua estrutura interna, mas os modelos tentam recriar este átomo. Nesse contexto, o modelo atômico de
A) Dalton defende que o átomo era uma estrutura maciça e indestrutível, mas poderia ser dividida em uma reação de fissão nuclear, por exemplo.
B) Thomson propõe um átomo neutro divido em duas regiões com partículas positivas e negativas.
C) Chadwick organiza o núcleo com duas partículas: prótons, com carga neutra, e nêutrons, com carga positiva.
D) Rutheford propõe a divisão do átomo em duas regiões: núcleo e eletrosfera, após realizar o experimento da lâmina de ouro.
E) Bohr organiza os elétrons em níveis de energia na eletrosfera, definindo que quanto mais próximo do núcleo os elétrons se encontram, mais energia eles possuem.
QUESTÃO 05
CRESPE 2021: A Tabela Periódica aumenta sua família de elementos com quatro nomes adicionais. Em sua sétima fila, foram incluídos oficialmente quatro novos inquilinos: os elementos 113, 115, 117 e 118 foram batizados como nihônio, moscóvio, tennessino e oganessono, respectivamente. O primeiro deles foi descoberto por cientistas do Instituto Riken no Japão; os outros, por equipes de cientistas da Rússia e dos Estados Unidos, todos eles integrados à Tabela Periódica desde janeiro.
Internet: <brasil.elpais.com> (com adaptações).
A esse respeito, assinale a opção correta.
A) Os quatro elementos descobertos estão localizados no sétimo período da Tabela Periódica e apresentam oito elétrons na camada de valência.
B) Os quatro elementos descobertos são classificados como cisurânicos, já que apresentam número atômico maior que 92.
C) O nihônio pertence à família dos calcogênios na Tabela Periódica.
D) O subnível mais energético do moscóvio é o 7p³.
E) O organessono é classificado como gás nobre e compõe o ar atmosférico.
QUESTÃO 06
CRESPE 2021: A figura precedente representa 4 sistemas formados por moléculas, em que bolinhas de cores diferentes representam átomos de elementos diferentes, e bolinhas juntas, que os átomos estão ligados entre si. Assinale a opção correta, de acordo com essa figura.
A) Considerando as substâncias no estado gasoso, o sistema 1 pode ser classificado como uma mistura heterogênea.
B) Os sistemas 2 e 4 são classificados como misturas.
C) O sistema 2 pode representar a molécula de CO2, que possui geometria linear.
D) O sistema 1 é classificado como mistura de duas substâncias compostas.
E) O sistema 3 pode representar uma molécula binária.
QUESTÃO 07
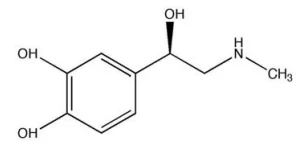
CRESPE 2021: A adrenalina, também conhecida como epinefrina, é um hormônio liberado na corrente sanguínea que tem a função de atuar sobre o sistema cardiovascular e manter o corpo em alerta para situações de fortes emoções ou estresse, como luta, fuga, excitação ou medo.
Internet: <www.tuasaude.com/adrenalina>.
Considerando-se a fórmula estrutural da adrenalina, representada na figura precedente, é correto afirmar que o número de ligações sigma e pi presentes em uma molécula de adrenalina corresponde, respectivamente, a
A) 13 e 3.
B) 23 e 3.
C) 28 e 4.
D) 24 e 3.
E) 26 e 3.
QUESTÃO 08
CRESPE 2021: Em reações químicas, o oxigênio pode reduzir a água oxigenada, que é uma solução aquosa de peróxido de hidrogênio — H2O2 (aq). As reações de oxirredução que envolvem a água oxigenada como reagente constituem casos particulares de reações, pois essa solução pode atuar como agente oxidante e também como redutor.
CrCl3 (aq) + H2O2 (aq) + NaOH (aq) → Na2CrO4 (aq) +
NaCl (aq) + H2O (l)
Internet: <www.ufjf.br/química> (com adaptações).
A respeito da reação de oxirredução não balanceada citada no texto acima, assinale a opção correta.
A) A reação em tela pode ser classificada como uma auto-oxirredução.
B) A água oxigenada é redutor na reação.
C) Considerando a reação balanceada com os menores coeficientes estequiométricos inteiros, a semirreação de redução da água oxigenada envolve três elétrons.
D) A soma dos menores coeficientes estequiométricos inteiros dessa equação é 31.
E) O número de oxidação do oxigênio na molécula de água oxigenada é −½.
QUESTÃO 09
CRESPE 2021: A glicose (C6H12O6) é o principal carboidrato encontrado no sangue. A taxa considerada normal é de 0,70 mg/mL a 1,10 mg/mL no sangue. Valores abaixo de 0,70 mg/mL caracterizam uma pessoa com hipoglicemia e, quando esse parâmetro é superior a 1,10 mg/mL, a pessoa está com hiperglicemia.
A partir dessa informação, considere que uma pessoa com massa corporal de 70 kg tenha doado sangue em um hemocentro. Sabendo-se que M (C6H12O6) = 180 g/mol, que o volume retirado de sangue correspondeu a 9 mL/kg e que o nível de glicose nesse sangue é de 0,80 mg/mL, é correto afirmar que foram doados por este paciente
A) 5,04 ⨯ 10⁻⁴ mol de glicose.
B) 2,8 ⨯ 10⁻² mol de glicose.
C) 6,3 ⨯ 10⁻⁴ mol de glicose.
D) 1,8 ⨯ 10⁻³ mol de glicose.
E) 2,8 ⨯ 10⁻³ mol de glicose.
QUESTÃO 10
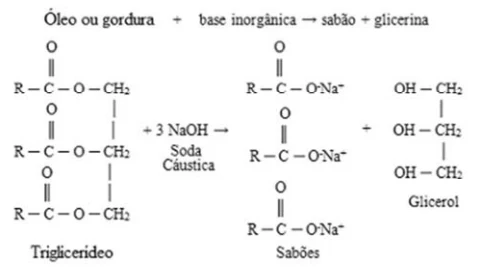
CRESPE 2021: Os primeiros sabões eram feitos com misturas de gorduras de animais (sebo), como o material graxo, com as cinzas de madeira, que possuem substâncias alcalinas, como o carbonato de sódio e de potássio. A seguir, é apresentado um exemplo de reação de saponificação.
Internet: <www.manualdaquimica.com> (com adaptações).
Com relação à reação de saponificação mostrada no texto anterior, assinale a opção correta.
A) A soda cáustica é uma base inorgânica classificada como forte e utilizada para produção de sabões insolúveis em água.
B) O triglicerídeo é um exemplo de éster muito solúvel em água.
C) Sabões são classificados como moléculas anfóteras, porque são capazes de se dissolver em meios polares e apolares.
D) O glicerol é um diálcool muito solúvel em água.
E) A reação de saponificação é um exemplo de uma hidrólise alcalina.
QUESTÃO 11
CRESPE 2021: A festa da virada de ano (réveillon) é marcada pela queima de fogos de artifício. No Brasil, o maior espetáculo acontece na praia de Copacabana, no Rio de Janeiro, mas este ano o evento foi cancelado por causa da pandemia. A explosão de cores no céu causada pela queima dos fogos é decorrente de um fenômeno que acontece com os elétrons dentro dos átomos, que, por sua vez, pode ser explicado pelo modelo atômico de Bohr que
A) afirma ocorrerem transições eletrônicas entre os níveis de energia, ou seja, o elétron libera fótons ao saltar de um nível mais interno para um nível mais externo.
B) define o fenômeno do salto quântico, em que os elétrons, ao absorverem energia, podem realizar um salto de um nível mais interno para um mais externo e, ao retornar para o nível de origem, liberar essa energia na forma de luz.
C) defende a ideia de que os elétrons de movimentam ao redor do núcleo com perda de energia, esta perda acontece com emissão de fótons.
D) quantifica a energia dentro da eletrosfera do átomo e afirma que o elétron libera luz ao saltar para um nível mais externo.
E) atribui as diferentes cores formadas pelos fogos de artifício ao fato de que a quantidade de energia liberada em todas as transições eletrônicas é a mesma, independentemente do nível de energia em que o elétron se encontre.
Texto 10A2-I
A exposição à radiação ultravioleta pode causar queimadura na pele, lesão em células epiteliais, alteração do DNA, inflamação, dilatação dos vasos sanguíneos, câncer, entre outros fatores adversos. O ozônio (O3) existente na estratosfera atua como um filtro dos raios ultravioletas provenientes do Sol.
Antigamente, muitos sprays utilizavam clorofluorcarbonos (CFCs) em sua composição. Esses CFCs ficavam na atmosfera e reagiam com o ozônio, decompondo-o.
Em 1989, foi assinado um acordo internacional denominado Protocolo de Montreal, por meio do qual mais de 130 países, incluído o Brasil, comprometeram-se a eliminar progressivamente o uso dessas substâncias em sprays e outras aplicações.
Um dos CFCs mais comuns possui fórmula CF2Cl2. Na estratosfera, sob luz ultravioleta, ele sofre a seguinte reação.
CF2Cl2 → •CF2Cl + Cl•
O átomo livre de cloro (Cl•), por sua vez, pode desencadear uma cascata de reações, como, por exemplo, as apresentadas a seguir.
O3 (g) + Cl• (g) → O2 (g) + ClO• (g)
O3 (g) + ClO• (g) → 2 O2 (g) + Cl• (g)
QUESTÃO 12
CRESPE 2021: Com base nas informações do texto 10A2-I, é correto afirmar que a ação da radiação ultravioleta sobre o CF2Cl2 se deve
A) à atividade catalítica.
B) ao efeito da temperatura.
C) à fotólise.
D) à diminuição da energia de ativação.
E) ao aumento da eficácia das colisões.
QUESTÃO 13
CRESPE 2021: Ainda a partir do texto 10A2-I, é correto afirmar que o mecanismo de reação apresentado entre a espécie química Cl• e o O3 é um exemplo de
A) reação de substituição.
B) catálise homogênea.
C) catálise heterogênea.
D) reação de dupla troca.
E) reação de simples troca.
QUESTÃO 14
CRESPE 2021: As substâncias A, B e C reagem entre si, produzindo as substâncias D e E. A velocidade inicial dessa reação foi medida para várias concentrações iniciais de A, B e C, à temperatura constante, e os resultados obtidos são os mostrados na seguinte tabela.
Com relação à situação hipotética precedente, assumindo-se v como a velocidade da reação e k como a constante de velocidade, é correto afirmar que a lei de velocidade dessa reação é dada por
A) v = k[A][B][C].
B) v = k[A][B]²[C].
C) v = k[A][B][C]².
D) v = k[A]²[B][C]².
E) v = k[A]²[B][C].
QUESTÃO 15
CRESPE 2021: Alguns povos indígenas da Amazônia utilizam a casca da quina (Coutarea hexandra) para extrair quinina, uma substância que eles utilizam para tratar febre. Atualmente, a quinina é utilizada no tratamento da malária e de arritmias cardíacas, além de ser o flavorizante da água tônica.
Os estudos sobre a cinética de degradação da quinina por ácido estabeleceram que a lei de velocidade dessa reação é dada por v = k [quinina] [ácido]², em que v é a velocidade da reação e k é a constante de velocidade. Nesses estudos, quando 1,0 × 10⁻⁴ mol/L de quinina foram misturados com 5,0 × 10⁻³ mol/L de ácido, a velocidade da reação medida foi de 2,4 × 10⁻³ mol·L⁻¹·s⁻¹.
Com base nessas informações, é correto afirmar que, se as concentrações iniciais de quinina e de ácido forem, respectivamente, de 0,250 mol/L e 0,160 mol/L, então a velocidade inicial da reação será igual a
A) 6,14 × 10³ mol∙L⁻¹∙s⁻¹.
B) 192 mol∙L⁻¹∙s⁻¹.
C) 30,72 mol∙L⁻¹∙s⁻¹.
D) 3,84 × 10⁴ mol∙L⁻¹∙s⁻¹.
E) 9,60 × 10⁵ mol∙L⁻¹∙s⁻¹.
QUESTÃO 16
CRESPE 2021: O gás NO reage com o gás O3 conforme a seguinte equação.
NO (g) + O3 (g) ⇌ NO2 (g) + O2 (g)
Estudos mostraram que, quando esses dois gases são colocados em um mesmo recipiente a 25 °C e 1 atm, cada molécula colide, em média, cerca de um bilhão de vezes por segundo com outras moléculas. Se todas essas colisões resultassem em formação de produto, a reação aconteceria em uma fração de segundo. Porém, não é isso que se observa empiricamente, sendo a reação muitíssimo mais lenta.
Nesse caso, para que a reação aconteça, a simples colisão entre as moléculas não é suficiente; é necessário, também, que
A) um catalisador seja adicionado ao meio reacional.
B) a colisão seja elástica e a massa de cada produto seja igual à massa de cada um dos reagentes.
C) as moléculas colidam com energia potencial superior à energia de ativação.
D) as moléculas colidam entre si com geometria favorável à formação do complexo ativado e com energia cinética suficiente.
E) a energia de ativação da reação seja diminuída.
Texto 10A2-II
O álcool estearílico é usado na indústria de cosméticos para a produção de cremes, loções, máscaras capilares, entre outros, por ser compatível com vários tipos de emulsionantes e apresentar baixa irritabilidade na pele.
Devido a um problema técnico em uma das indústrias de produção desse insumo, esse produto passou a ficar escasso no mercado, o que levou uma indústria de cosméticos a considerar o estearato de metila como possível alternativa para a produção do álcool estearílico, a partir da hidrogenação do estearato de metila, em solução de heptano, por meio da seguinte reação.
C19H38O2(sol) + 2 H2 (g) → C18H37OH(sol) + CH3OH(sol)
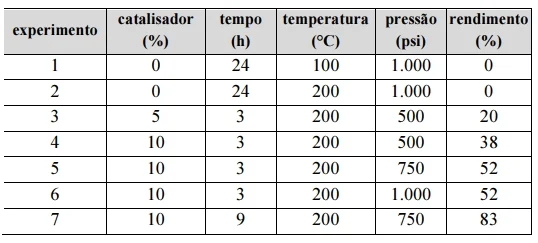
A planta piloto dessa indústria de cosméticos é equipada com um reator do tipo autoclave, que opera em temperatura máxima de 200 °C e pressão máxima de 1.000 psi e que pode ser utilizado para desenvolver o projeto. Para que a síntese do álcool estearílico seja bem-sucedida, o químico resolveu testar várias condições reacionais, a fim de descobrir qual delas proporcionará a obtenção de maior quantidade de álcool estearílico (rendimento) no menor tempo possível. Ele testou diversas condições experimentais, tais como tempo de reação, temperatura e pressão do reator, além de um catalisador comercial à base de cobre. Os resultados dos testes são mostrados na tabela a seguir. Sabe-se que o hidrogênio molecular (H2) é instável a temperaturas acima de 200 °C.
QUESTÃO 17
CRESPE 2021: Considerando a situação hipotética apresentada no texto 10A2-II, assinale a opção correta, no que diz respeito ao catalisador.
A) A adição de catalisador aumentou a velocidade da reação, porém a uma taxa muito pequena para as finalidades industriais.
B) O catalisador deslocou o equilíbrio da reação para a direita, conforme o princípio de Le Châtelier.
C) O catalisador é dispensável nessa síntese, pois é possível obter bons rendimentos de reação apenas se ajustando a temperatura e a pressão.
D) O uso de catalisador é imperativo nesse caso, uma vez que a energia de ativação dessa reação é alta e não é possível trabalhar em temperaturas ainda mais altas.
E) O catalisador aumentou a velocidade da reação, porque aumentou a superfície de contato entre os reagentes.
QUESTÃO 18
CRESPE 2021: No que tange ao efeito da pressão na situação hipotética apresentada no texto 10A2-II, julgue os itens a seguir.
I O aumento da pressão aumentou a velocidade da reação até atingir o limite desse parâmetro, pois, com o aumento da pressão de H2, mais hidrogênio foi dissolvido na solução.
II O aumento da pressão aumentou a velocidade da reação, o que comprova que a reação é de 1.ª ordem em relação ao hidrogênio.
III O fato de haver um limite para o aumento da velocidade da reação devido à pressão indica que existe uma capacidade limitada do catalisador de suportar o H2.
Assinale a opção correta.
A) Nenhum item está certo.
B) Apenas o item II está certo.
C) Apenas o item III está certo.
D) Apenas os itens I e II estão certos.
E) Apenas os itens I e III estão certos.
QUESTÃO 19
CRESPE 2021: Na situação hipotética apresentada no texto 10A2-II, se o hidrogênio fosse estável a temperaturas acima de 200 °C, seria de se esperar que o aumento da temperatura do meio
A) diminuísse o rendimento da reação, devido ao aumento da energia de ativação da reação.
B) aumentasse o rendimento da reação, devido ao aumento da energia cinética das moléculas.
C) aumentasse o rendimento da reação, devido à diminuição da energia de ativação da reação.
D) não alterasse o rendimento da reação.
E) diminuísse o rendimento da reação, devido à combustão do estearato de metila.
QUESTÃO 20
CRESPE 2021: A água do mar é um eletrólito, devido à alta concentração de sal, e eletrólitos causam corrosão em metais. Cascos de navios podem sofrer toda sorte de processos corrosivos eletroquímicos, tais como aeração diferencial, corrosão atmosférica e corrosão eletrolítica.
A fim de evitar essa deterioração do casco, as companhias navais utilizam revestimentos protetores, tais como tintas, lacas, esmaltes, vernizes, resinas, dispersões, emulsões, óleos protetores e recoberturas. Esses revestimentos protegem o casco do navio porque
A) reagem com o ferro, produzindo Fe2O3, que, por sua vez, protege o casco do navio contra a corrosão.
B) contêm em sua composição uma substância inibidora da oxidação do ferro.
C) contêm em sua composição uma substância que se oxida primeiramente que o ferro, o que previne a oxidação do metal.
D) possuem menor potencial de redução que o ferro, sendo, portanto, sacrificados para proteger o casco.
E) reduzem a superfície de contato do casco com a água e com o oxigênio.
QUESTÃO 21
CRESPE 2021: Um suco de laranja estraga muito mais rapidamente que a fruta propriamente dita. Isso ocorre porque
A) a vitamina C presente na laranja ativa o oxigênio atmosférico e age como catalisador da oxidação do suco.
B) a concentração de O2 no suco dentro da laranja intacta é muito mais baixa que no suco extraído da fruta.
C) o ar atmosférico contém microrganismos decompositores que não conseguem penetrar a casca da laranja.
D) a concentração de CO2 no suco dentro da laranja intacta é muito mais alta que no suco extraído da fruta.
E) o oxigênio atmosférico funciona como catalisador da degradação do suco extraído da laranja.
QUESTÃO 22
CRESPE 2021: O esomeprazol, cuja estrutura química está representada na figura seguinte, é um agente inibidor da bomba de prótons, com ação no controle da secreção de ácido gástrico.
Considerando-se a estrutura química do esomeprazol, bem como M(H) = 1,00 g/mol, M(C) = 12,00 g/mol, M(N) = 14,00 g/mol, M(O) = 16,00 g/mol e M(S) = 32,00 g/mol, é correto afirmar que sua fórmula molecular e sua massa molar são, respectivamente,
A) C17H17N3O3 e 311 g/mol.
B) C17H19N2O3S e 331 g/mol.
C) C16H17N3O2S e 315 g/mol.
D) C17H19N3O3S e 345 g/mol.
E) C16H18N3O3S e 332 g/mol.
QUESTÃO 23
CRESPE 2021: A figura a seguir mostra a estrutura química do remdesivir, um profármaco de ação antiviral de amplo espectro, com atividade in vitro observada contra diversos vírus de RNA, tais como o ebola, o MERS-CoV e o SARS-CoV. Ele atua como um inibidor de RNA polimerase dependente de RNA, comprometendo o processo de replicação do genoma viral.
De acordo com a estrutura química apresentada, é correto afirmar que os grupos funcionais do remdesivir incluem
A) amina, éster e cetona.
B) amida, amina e éter.
C) álcool, amida e ácido carboxílico.
D) aldeído, éter e amina.
E) amina, álcool e éster.
QUESTÃO 24
CRESPE 2021: A próxima figura representa a estrutura química da teriflunomida, um agente imunomodulador e anti-inflamatório utilizado no tratamento de primeira linha de pacientes com esclerose múltipla.
Na estrutura química da teriflunomida, existem
A) 4 carbonos primários, 7 carbonos secundários e 1 carbono terciário.
B) 4 carbonos primários, 6 carbonos secundários e 2 carbonos terciários.
C) 3 carbonos primários, 7 carbonos secundários e 2 carbonos quaternários.
D) 3 carbonos primários, 7 carbonos secundários e 2 carbonos terciários.
E) 5 carbonos primários, 6 carbonos secundários e 1 carbono quaternário.
QUESTÃO 25
CRESPE 2021: Considerando as fórmulas químicas de ácidos, bases, óxidos e sais, assinale a opção que apresenta apenas fórmulas de compostos que podem ser obtidos em uma reação de neutralização total.
A) NaCl, Mg(NO3)2, NH4CN
B) FeO, NaCl, CO2
C) KF, CsCl, HNO3
D) CaCO3, PbS, NaOH
E) K2Cr2O7, HCN, CuSO4
QUESTÃO 26
CRESPE 2021: Em uma solução ácida,
A) a concentração de OH⁻ é igual a zero.
B) a constante de ionização da água, Kw, é igual a 1 × 10⁻⁷.
C) a concentração de OH⁻ é igual à concentração de H⁺.
D) o pH é negativo.
E) a concentração de H⁺ é maior que a concentração de OH⁻.
QUESTÃO 27
CRESPE 2021: Em uma solução com pH igual a 4, a concentração de íons OH⁻, em mol/L, é igual a
A) 10⁻⁸.
B) 10⁻⁹.
C) 10⁻¹⁰.
D) 10⁻¹¹.
E) 10⁻¹².
QUESTÃO 28
CRESPE 2021: Os equilíbrios representados pelas reações a seguir ocorrem quando o ácido fórmico (HCO2H) e a metilamina (CH3NH2) se dissolvem em água.
reação 1: HCO2H (l) + H2O (l) ⇌ H3O+ (aq) + HCO2–(aq)
reação 2: CH3NH2 (l) + H2O (l) ⇌ CH3NH3+ (aq) + OH– (aq)
A partir dessas informações, assinale a opção que apresenta os pares conjugados ácido/base para as reações 1 e 2, respectivamente, considerando a reação direta, ou seja, o reagente ácido e sua respectiva base conjugada.
A) HCO2⁻/HCO2H e CH3NH3⁺/CH3NH2
B) HCO2⁻/HCO2H e CH3NH2/CH3NH3⁺
C) HCO2H/HCO2⁻ e H2O/OH⁻
D) HCO2H/HCO2⁻ e CH3NH2/CH3NH3⁺
E) H2O/H3O⁺ e H2O/OH⁻
QUESTÃO 29
CRESPE 2021: Uma solução orgânica foi submetida a um feixe de luz polarizada. Entretanto, o plano de vibração dessa luz não sofreu desvio (rotação).
De acordo com aspectos da isomeria espacial, é correto afirmar que, na situação hipotética apresentada, pode ter sido utilizada uma solução com
A) 1 mol/L de (R)-2-butanol.
B) 1 mol/L de (R)-2-pentanol.
C) 1 mol/L de (S)-2-pentanol.
D) 2 mol/L de (R)-2-pentanol e 2 mol/L de (S)-2-pentanol.
E) 2 mol/L de (R)-2-butanol e 3 mol/L de (S)-2-butanol.
QUESTÃO 30
CRESPE 2021: Considerando a estrutura química da D-eritrose, apresentada na figura anterior, assinale a opção que contém o número total de estereoisômeros para essa molécula orgânica.
A) 2
B) 3
C) 4
D) 8
E) 16
QUESTÃO 31
CRESPE 2021: Assinale a opção em que o composto exibido apresenta isomeria cis-trans.
A) (CH3)2C=CCl−NH2
B) CH3−CH2−CH=CH−OH
C) CH2=CBr2
D) CH2=CH−Cl
E) (CH3−CH2)2C=C(CH2−CH3)2
QUESTÃO 32
CRESPE 2021: De acordo com a teoria ácido-base de Arrhenius, um ácido é
A) uma espécie que pode aceitar um par de elétrons.
B) uma substância que, ao sofrer ionização em meio aquoso, libera íons H⁺.
C) uma substância que, ao sofrer ionização em meio aquoso, libera íons OH⁻.
D) uma espécie química capaz de doar um próton.
E) uma espécie química capaz de receber um próton.















COMENTÁRIOS